PONAVLJANJE ZA PRVU PISANU PROVJERU ZNANJA
PONAVLJANJE ZA PRVU PISANU PROVJERU ZNANJA – KEMIJA 8
U sljedećim je zadatcima točan samo jedan odgovor. Zaokruži slovo ispred točnog odgovora.
1. Koja je od navedenih tvari pri sobnoj temperaturi u čvrstom agregacijskom stanju?
a) Brom B) jod c) dušik d) živa
1. Čije atome sadržavaju svi sulfidi?
a) Atome dušika b) atome kisika c) atome metala d) atome sumpora
2. Vodena otopina je kisela zbog prisutnosti:
a) Oksonijevih iona b) hidroksidnih iona c) kloridnih iona d) metiloranža
3. Što nastaje miješanjem kalcijeva oksida i vode?
b) Gašeno vapno b) kalcijev karbonat c) vodik d) živo vapno
4. Broj atoma u molekuli označavamo:
a) Indeksom b) koeficijentom c) eksponentom d) razlomkom
5. Kemijski spoj koji nije građen od iona je:
a) NaCl b) KBr c) HBr d) CaCl2
6. Jednak broj negativno nabijenih čestica kao atom argona ima:
a) anion klora b) anion c) anion fluora d) kation magnezija
U sljedećim zadacima točna s dva odgovora. Zaokruži slova ispred točnih odgovora.
7. Soli mogu nastati reakcijom:
a) Metala i kiselina b) kiseline i lužine
c) oksida nemetala i kiseline d) nemetala i kiseline
8. Što je karakteristično za sumporov(IV) oksid?
a) Ne reagira s vodom b) tekućina je pri sobnoj temperatutri
c) reagira s vodom dajući kiselinu d)otrovan je plin pri sobnoj temperaturi
9. U lužini će se promijeniti boja
a) Metiloranža b)fenolftaleina
c) plavog lakmus papira d) crvenog lakmus papira
Dopuni sljedeće tvrdnje riječima koje nedostaju.
10. Indikatorima za lužine dokazuje se prisutnost _________________ iona.
11. Oksidi nemetala su spojevi ______________ s ___________________.
12. Reagira li metal s klorovodičnom kiselinom nastaju __________________ i vodik.
13. Soli dušične kiseline nazivaju se ____________, a soli ugljične kiseline ___________.
14. Vodene otopine hidroksida nazivaju se ______________________ .
15. Uvođenjem sumporova(VI) oksida u vodu nastaje __________________ _________.
Za točnu tvrdnju zaokruži slovo T, a za netočnu slovo N.
16. Natrij je zemnoalkalijski metal. T N
17. Metali su dobri vodiči električne struje. T N
18. Reagens za dokazivanje ugljikova dioksida jest bakrov(II) sulfat. T N
19. Ugljična kiselina ima pH - vrijednost manju od 7. T N
20. Natrijev klorid, NaCl(s) provodi električnu struju. T N
21. Hrđanje željeza je fizikalna promjena. T N
22. Svi hidroksidi daju lužine. T N
23. Dovrši jednadžbe kemijskih reakcija.
a) ___SO2(g) + __ ____ (g) → __SO3(g)
b) ___ MgO(s) + __ HNO3(aq) → ___ _____(aq) + __ H2O(l)
24. Kvantitaivno opiši kemijske reakcije iz prethodnog zadatka.
a)
b)
25. Razvrstaj tvari u tablicu prema skupini spojeva kojoj pripradaju.
CuO, H3PO4, NaCl, CaS, SO3, CaO, NaOH, HCl, Ca(OH)2, CO
|
OKSIDI METALA |
OKSIDI NEMETALA |
HIDROKSID |
KISELINA |
SOL |
|
|
|
|
|
|
26. Upotpuni tablicu imenima ili formulama kemijskih spojeva.
|
IME SPOJA |
KEMIJSKA FORMULA |
|
|
FeCl2(s) |
|
Kalijev hidroksid |
|
|
|
H2CO3 (s) |
|
Kalcijev karbonat |
|
|
|
HCl(aq) |
|
|
HCl(g) |
|
Sumporov trioksid |
|
|
Sumporna kiselina |
|
27. Za svaki ponuđeni par atoma napiši tvore li zajedno molekulu ili formulsku jedinku:
a) vodik – vodik ________________________________
b) kalcij – kisik ________________________________
c) željezo – sumpor _______________________________
28. Popuni tablicu.
|
Oznaka kationa ili aniona |
Ime kationa ili aniona |
|
Br - |
|
|
|
Magnezijev ion |
|
O2- |
|
|
|
kalijev ion |
29. Popuni tablicu traženim podacima.
|
Kemijska simbolika |
Kvantitativno značenje |
|
3 N2 |
|
|
8 Cl |
|
|
3 H2O |
|
|
7 MgO |
|
30. Odredi valencije atoma u sljedećim spojevima tako da ih napišeš iznad svakog atoma i imenuj spojeve.
a) NO2 ___________ b) MgCl2 ___________________ c) NH3 ____________________
31. Zaokruži slovo ispred dvaju točnih odgovora. Jednak broj negativno nabijenih čestica kao fluoridni ion ima:
a) oksidni ion b) atom argona c) atom neona d) sulfidni ion e) magnezijev ion
32. Dovrši zadani izraz tako da nastane kation ili anion zadanog kemijskog elementa.
a) Al → _____ + _____ b) O + _____ → _____
33. Napiši empirijsku formulu ionskog spoja iz prethodnog zadatka.
34. Navedi dva čimbenika koji ubrzavaju hrđanje željeza.
PRIRODOZNANSTVENE KOMPETENCIJE
1. Popuni tablicu podacima koji nedostaju
|
ATOM |
N(p+) |
N(e-) |
N(n0) |
Z |
A |
|
Željezo |
|
|
30 |
|
|
|
Aluminij |
|
|
|
|
27 |
|
Kisik |
|
|
|
|
17 |
|
fluor |
|
|
10 |
|
|
2. Napiši broj protona i elektrona u zadanim ionima:
|
Vrsta iona |
N(p+) |
N(e-) |
|
N3- |
|
|
|
Na+ |
|
|
|
F- |
|
|
|
Mg2+ |
|
|
3. U jednom dijelu kristala aluminijeva klorida izbrojeno je 250 atoma aluminija i 750 atoma klora. Napiši formulsku jedinku spoja.
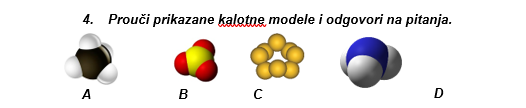
a) Koji modeli prikazuju modele molekula kemijskih spojeva?
b) Kojim slovom je označen model kemijskog spoja koji će u reakciji s vodom dati lužinu?
c) Napiši jednadžbu kemijske reakcije spoja iz prethodnog zadatka s vodom.
d) Koji modeli prikazuju modele molekula elementarnih tvari?
e) Koji model prikazuje kemijski spoj koji će reagirati s vodom iz zraka pri čemu će nastati kisele kiše?
f) Napiši kemijsku formulu modela kemijskog spoja iz prethodnog zadatka.
g) Napiši kemijsku formulu kemijskog spoja koji u svojoj građi ima atome vodika i atom ugljika.
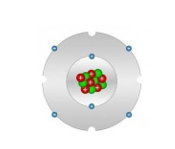
5. Prouči shematski prikaz atoma nekog kemijskog elementa i popuni tablicu traženim podacima.
|
IME ELEMENTA |
|
|
SIMBOL ELEMNTA |
|
|
REDNI BROJ |
|
|
BROJ PERIODE |
|
|
BROJ SKUPINE |
|
|
N(p+) |
|
|
N(e-) |
|
6. Skiciraj piktograme opasnosti koji se nalaze na etiketi boce u kojoj se nalazi sumporna kiselina i navedi njihovo značenje.
7. Marko je ispitivao električnu vodljivost ugljične i dušične kiseline. Digitalnim multimetrom je izmjerio da je I(dušične kiseline) = 7 µA, I(ugljične kiseline) = 0,9 µA.
a) Koja kiselina ima više slobodnih iona?
8. Jura je s unutarnje strane staklenog zvona pričvrstio plavi lakmus papir. Ispod staklenog zvona stavio je cvijet narančaste boje i svijeću koja gori. Nakon toga je zapalio sumpornu traku i stavio ju u tarionik ispod staklenog zvona. Nakon nekog vremena Jura je uočio da se svijeća ugasila, da je plavi lakmus papir promijenio boju u crvenu i da je boja cvijeta izblijedjela.
a) Što možeš zaključiti na temelju Jurinih opažanja?
b) Napiši jednadžbe kemijskih reakcija koje opisuju promjene koje su se dogodile tijekom pokusa.
(nemoj zaboraviti pisati agregacijska stanja tvari)
JKR 1:
JKR 2:
c) Tvar koja je nastala gorenjem sumpora je otrovna. Na temelju opažanja i zaključka iz zadatka a napiši čime ćeš neutralizirati djelovanje te tvar.
d) Napiši jednadžbu kemijske reakcije koja će potkrijepiti tvoj odgovor iz prethodnog zadatka. (nemoj zaboraviti pisati agregacijska stanja tvari)
JKR:
9. Prouči grafikon i odgovori na pitanja.
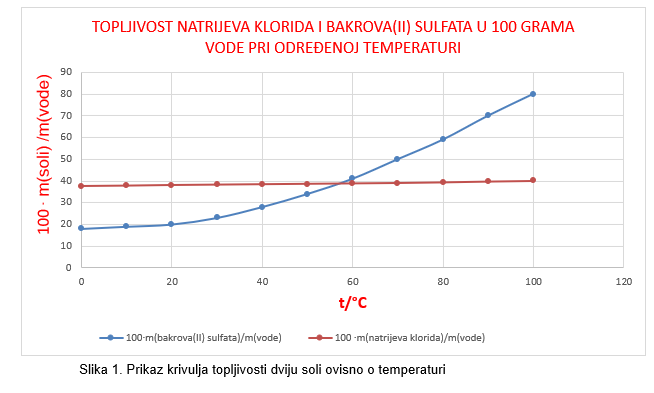
a) Kojoj soli se topljivost slabo povećava s porastom temperature?
b) Napiši kemijsku formulu te soli.
c) Pri kojoj temperaturi je topljivost tih dviju soli jednaka?
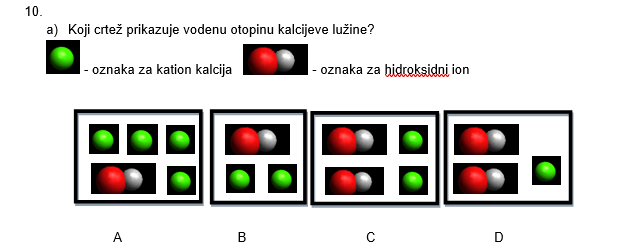
b) Prikaži jednažbom kemijske reakcije disocijaciju kalcijeve lužine.(označi
agregacijska stanja tvari)
c)Što će se dogoditi s brojem hidroksidnih iona i pH-vrijednošću vodene otopine kalcijeve lužine ako
u nju dodamo nekoliko kapi vodne otopine klorovodične kiseline?
